INTRODUCCIÓN Y OBJETIVOS.
Actualmente según datos del Grupo de Estudio de Enfermedades Cerebrovasculares de la Sociedad Española de Neurología (GEECV-SEN) se detectan anualmente unos 130.000 ictus y 40.000 personas al año mueren en España por culpa de esta enfermedad que constituye actualmente uno de los problemas socio-sanitarios más importantes y que precisa de estrategias concretas para su manejo y control.
Multiples estudios multicentricos, prospectivos,randomizados (MR CLEAN, ESCAPE, EXTEND IA, SWIFT PRIME ,REVASCAT, THRACE Y PISTE ) han demostrado desde el 2015, un significativo beneficio de la terapia endovascular con trombectomía mecánica respecto al mejor tratamiento médico en el ictus agudo secundario a una oclusión de gran vaso.
Un Centro de tratamiento del ictus agudo debe disponer tener la disponibilidad 24 horas al día, 7 días a la semana, 365 días al año de TAC y Angiotac (o RM y Angiorm ) y de profesionales capaces del análisis de las imágenes que permitan una adecuada selección de los pacientes para aplicar un tratamiento de reperfusión.
Las técnicas avanzadas de imagen permiten demostrar la oclusión de un vaso de mediano o gran calibre y pueden, aunque todavía está por probarse con nivel de evidencia significativo, aportar una importante información sobre el volumen de infarto establecido y el potencial tejido cerebral en riesgo pero salvable con una revascularización precoz, que nos permita establecer mejor la indicación del tratamiento endovascular.
Esta selección por técnicas de imagen avanzada puede ser especialmente útil en pacientes con una ventana temporal desde el inicio de los síntomas superior a las 6-8 horas, incluyendo los ictus del despertar o de origen desconocido, ictus con oclusión proximal y deficit neurológico menor fluctuante, pacientes con ictus establecido de gran tamaño con ASPECTS < 6, oclusiones extracraneales aisladas, pacientes de más de 80-85 años….
Nuestro objetivo es la descripción de las técnicas de imagen más utilizadas para la selección del tratamiento en pacientes con un ictus agudo , sus ventajas y desventajas.
EXPOSICIÓN
- TC craneal simple y angioTC
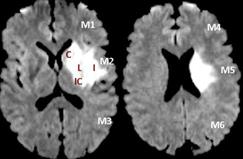
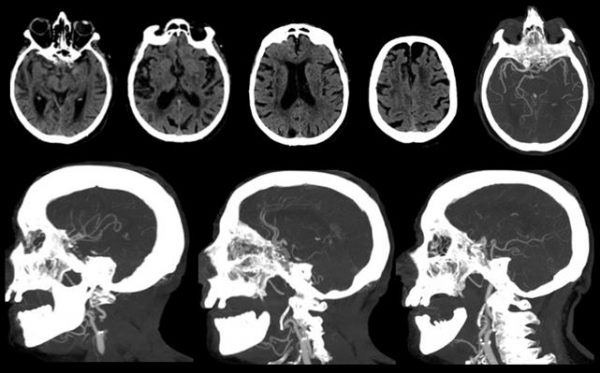
Son de rápida adquisición, económicas y ampliamente disponibles. El TC simple permite descartar de forma la presencia de hemorragia y determinar los signos incipientes de isquemia aguda. El angioTC permite valorar la presencia de oclusión arterial tras la administración de un medio de contraste. De este modo estimamos el tejido en riesgo como aquel situado más allá de la oclusión arterial. Si el TC simple muestra una relativa integridad del parénquima, es decir, el core es pequeño y en el angioTC se visualiza una oclusión de gran arteria podemos extrapolar que existe mismatch por lo que el paciente sería candidato a tratamiento de revascularización arterial. Las limitaciones de esta técnica son la alta variabilidad interobservador para la identicación de signos incipientes de isquemia en especial cuando la neuroimagen se realiza dentro de los primeros minutos desde el inicio de los síntomas y la baja sensibilidad del TC simple para la detección de isquemia cerebral aguda.
- TC perfusión: esta técnica permite la creación de mapas de flujo, tiempo y volumen tras la administración de contraste intravenoso y a través de algoritmos previamente definidos. De acuerdo a umbrales predefinidos se identica el mismatch como la ratio entre el tejido afecto en mapas de flujo y el tejido afecto en mapas de volumen. Las ventajas del TC perfusión son la rápida adqui- sición (entre 60 y 90 segundos) y la obtención de una medida cuantitativa del tejido con daño irreversible y del tejido en riesgo. En cuanto a sus limitaciones, se trata de una técnica que expone al paciente a radiación, generalmente tiene una cobertura cerebral limitada y tanto la metodología de la adquisición como del análisis posterior es heterogénea.
- RM multimodal: incluye la realización de al menos una secuencia eco de gra-diente (permite descartar la presencia de hemorragia intracraneal), una secuencia de difusión (DWI), un estudio angioRM y un estudio de perfusión (PWI). La secuencia de difusión es la técnica más precisa en este momento para la identicación del core isquémico. La angioRM permite valorar el lugar de la oclusión y la secuencia de perfusión, de manera similar al TC perfusión, genera mapas de ujo, tiempo y volumen tras la administración de gadolinio intravenoso. El mismatch se calcula como la ratio entre el volumen de tejido afecto en DWI y el volumen de tejido con un retraso en los mapas de tiempo (TMax>6segundos). Las ventajas de la RM multimodal incluyen una mayor precisión en la identificación del core desde estadios muy precoces. En cuanto a sus limitaciones, la adquisición y el tiempo provocan un alargamiento de los tiempos puerta-intervención terapéutica. Además, se trata de una técnica más sujeta a los movimientos del paciente y que permite una peor monitorización de los pacientes inestables.
BIBLIOGRAFÍA
- Campbell BCV, Mitchell PJ, Kleinig TJ, Dewey HM, Churilov L, Yassi N, Yan B, Dowling RJ, Parsons MW, Oxley TJ, Wu TY, Brooks M, Simpson MA, Miteff F, Levi CR, Krause M, Harrington TJ, Faulder KC, Steinfort BS, Priglinger M, Ang T, Scroop R, Barber PA, McGuinness B, Wijeratne T, Phan TG, Chong W, Chandra RV, Bladin CF, Badve M, Rice H, de Villiers L, Ma H, Desmond PM, Donnan GA, Davis SM, EXTEND- IA Investigators. Endovascular therapy for ischemic stroke with perfusion-imaging selection. Engl. J. Med. 2015;372:1009–1018.
- Saver JL, Goyal M, Bonafe A, Diener H-C, Levy EI, Pereira VM, Albers GW, Cog- nard C, Cohen DJ, Hacke W, Jansen O, Jovin TG, Mattle HP, Nogueira RG, Siddi- qui AH, Yavagal DR, Baxter BW, Devlin TG, Lopes DK, Reddy VK, Mesnil de Rochemont du R, Singer OC, Jahan R, SWIFT PRIME Investigators. Stent-retriever thrombectomy after intravenous t-PA vs. t-PA alone in stroke. Engl. J. Med. 2015;372:2285–2295.
- Goyal M, Demchuk AM, Menon BK, Eesa M, Rempel JL, Thornton J, Roy D, Jovin TG, Willinsky RA, Sapkota BL, Dowlatshahi D, Frei DF, Kamal NR, Montanera WJ, Poppe AY, Ryckborst KJ, Silver FL, Shuaib A, Tampieri D, Williams D, Bang OY, Baxter BW, Burns PA, Choe H, Heo J-H, Holmstedt CA, Jankowitz B, Kelly M, Li- nares G, Mandzia JL, Shankar J, Sohn S-I, Swartz RH, Barber PA, Coutts SB, Smith EE, Morrish WF, Weill A, Subramaniam S, Mitha AP, Wong JH, Lowerison MW, Sajobi TT, Hill MD, ESCAPE Trial Investigators. Randomized assessment of rapid endovascular treatment of ischemic stroke. Engl. J. Med. 2015;372:1019–1030.
- Jovin TG, Chamorro A, Cobo E, de Miquel MA, Molina CA, Rovira A, San Román L, Serena J, Abilleira S, Ribó M, Millán M, Urra X, Cardona P, López-Cancio E, Tomasello A, Castaño C, Blasco J, Aja L, Dorado L, Quesada H, Rubiera M, Her- nandez-Pérez M, Goyal M, Demchuk AM, Kummer von R, Gallofré M, Dávalos A, REVASCAT Trial Investigators. Thrombectomy within 8 hours after symptom onset in ischemic stroke. Engl. J. Med. 2015;372:2296–2306.
- Berkhemer OA, Fransen PSS, Beumer D, van den Berg LA, Lingsma HF, Yoo AJ, Schonewille WJ, Vos JA, Nederkoorn PJ, Wermer MJH, van Walderveen MAA, Staals J, Hofmeijer J, van Oostayen JA, Lycklama à Nijeholt GJ, Boiten J, Brouwer PA, Emmer BJ, de Bruijn SF, van Dijk LC, Kappelle LJ, Lo RH, van Dijk EJ, de Vries J, de Kort PLM, van Rooij WJJ, van den Berg JSP, van Hasselt BAAM, Aerden LAM, Dallinga RJ, Visser MC, Bot JCJ, Vroomen PC, Eshghi O, Schreuder THCML, Heijboer RJJ, Keizer K, Tielbeek AV, Hertog den HM, Gerrits DG, van den Berg- Vos RM, Karas GB, Steyerberg EW, Flach HZ, Marquering HA, Sprengers MES, Jenniskens SFM, Beenen LFM, van den Berg R, Koudstaal PJ, van Zwam WH, Roos YBWEM, van der Lugt A, van Oostenbrugge RJ, Majoie CBLM, Dippel DWJ, MR CLEAN Investigators. A randomized trial of intraarterial treatment for acute ischemic stroke. Engl. J. Med. 2015;372:11–20.
- Bracard S, Ducrocq X, Mas J-L, Soudant M, Oppenheim C, Moulin T, Guillemin F, THRACE investigators. Mechanical thrombectomy after intravenous alteplase versus alteplase alone after stroke (THRACE): a randomised controlled trial. Lan- cet Neurol. 2016;15:1138–1147.
- Muir KW, Ford GA, Messow C-M, Ford I, Murray A, Clifton A, Brown MM, Madi- gan J, Lenthall R, Robertson F, Dixit A, Cloud GC, Wardlaw J, Freeman J, White P, PISTE Investigators. Endovascular therapy for acute ischaemic stroke: the Prag- matic Ischaemic Stroke Thrombectomy Evaluation (PISTE) randomised, contro- lled trial. J. Neurol. Neurosurg. Psychiatr. 2017;88:38–44.
- Goyal M, Menon BK, van Zwam WH, Dippel DWJ, Mitchell PJ, Demchuk AM, Dávalos A, Majoie CBLM, van der Lugt A, de Miquel MA, Donnan GA, Roos YBWEM, Bonafe A, Jahan R, Diener H-C, van den Berg LA, Levy EI, Berkhemer OA, Pereira VM, Rempel J, Millán M, Davis SM, Roy D, Thornton J, Román LS, Ribó M, Beumer D, Stouch B, Brown S, Campbell BCV, van Oostenbrugge RJ, Saver JL, Hill MD, Jovin TG, HERMES collaborators. Endovascular thrombectomy after large-vessel ischaemic stroke: a meta-analysis of individual patient data from ve randomised trials. Lancet. 2016;
- Powers WJ, Derdeyn CP, Biller J, Coffey CS, Hoh BL, Jauch EC, Johnston KC, Johnston SC, Khalessi AA, Kidwell CS, Meschia JF, Ovbiagele B, Yavagal DR. 2015 American Heart Association/American Stroke Association Focused Update of the 2013 Guidelines for the Early Management of Patients With Acute Ische- mic Stroke Regarding Endovascular Treatment A Guideline for Healthcare Pro- fessionals From the American Heart Association/American Stroke Association. Stroke. 2015;46:3020– 3035.
- Wardlaw JM, Mielke O. Early signs of brain infarction at CT: observer reliabi- lity and outcome after thrombolytic treatment–systematic review. Radiology. 2005;235:444–453.
- Wheeler HM, Mlynash M, Inoue M, Tipirneni A, Liggins J, Zaharchuk G, Straka M, Kemp S, Bammer R, Lansberg MG, Albers GW, DEFUSE 2 Investigators. Early diffusion-weighted imaging and perfusion-weighted imaging lesion volumes forecast nal infarct size in DEFUSE 2. Stroke. 2013;44:681–685.
- Chalela JA, Kidwell CS, Nentwich LM, Luby M, Butman JA, Demchuk AM, Hill MD, Patronas N, Latour L, Warach S. Magnetic resonance imaging and computed tomography in emergency assessment of patients with suspected acute stroke: a prospective comparison. The Lancet. 2007;369:293–298.
- Campbell BCV, Yassi N, Ma H, Sharma G, Salinas S, Churilov L, Meretoja A, Par- sons MW, Desmond PM, Lansberg MG, Donnan GA, Davis SM. Imaging selection in ischemic stroke: feasibility of automated CT-perfusion analysis. International Journal of Stroke. 2014;10:51–54.
- Hill MD, Rowley HA, Adler F, Eliasziw M, Furlan A, Higashida RT, Wechsler LR, Roberts HC, Dillon WP, Fischbein NJ, Firszt CM, Schulz GA, Buchan AM, PROACT- II Investigators. Selection of acute ischemic stroke patients for intra-arterial thrombolysis with pro-urokinase by using ASPECTS. Stroke. 2003;34:1925–1931.
- Demchuk AM, Hill MD, Barber PA, Silver B, Patel SC, Levine SR, NINDS rtPA Stroke Study Group, NIH. Importance of early ischemic computed tomography changes using ASPECTS in NINDS rtPA Stroke Study. Stroke. 2005;36:2110–2115.
- Dzialowski I, Hill MD, Coutts SB, Demchuk AM, Kent DM, Wunderlich O, Kum- mer von R. Extent of early ischemic changes on computed tomography (CT) before thrombolysis: prognostic value of the Alberta Stroke Program Early CT Score in ECASS II. Stroke. 2006;37:973–978.
- Hill MD, Demchuk AM, Goyal M, Jovin TG, Foster LD, Tomsick TA, Kummer von R, Yeatts SD, Palesch YY, Broderick JP, IMS3 Investigators. Alberta Stroke Program early computed tomography score to select patients for endovas- cular treatment: Interventional Management of Stroke (IMS)-III Trial. Stroke. 2014;45:444–449.